在腦瘤治療領域,特別是針對膠質母細胞瘤(#Glioblastoma, GBM),#CAR-T細胞療法始終面臨兩大挑戰:腫瘤細胞的高度異質性(tumor heterogeneity)與免疫細胞難以深入腫瘤微環境(tumor microenvironment, TME)發揮作用。發表於《Advanced Science》的研究,提出一套名為「prof 雞尾酒療法」的創新策略,結合多靶點設計、γδ T細胞工程化與病患衍生 #腫瘤類器官(GBM organoids, GBOs)驗證,為個人化CAR-T療法開啟新局。
🔬 研究背景:CAR-T療法在固態腫瘤的瓶頸
雖然CAR-T細胞在血液腫瘤中表現亮眼,但在GBM等固態腫瘤中,臨床反應仍不理想。原因之一是GBM細胞表面抗原表現高度異質,單一靶點CAR-T細胞容易因「抗原逃逸」(antigen escape)而失效。此外,GBM的TME富含免疫抑制因子,抑制T細胞的滲透與殺傷能力。
🧠 關鍵創新:prof 雞尾酒療法的三大支柱
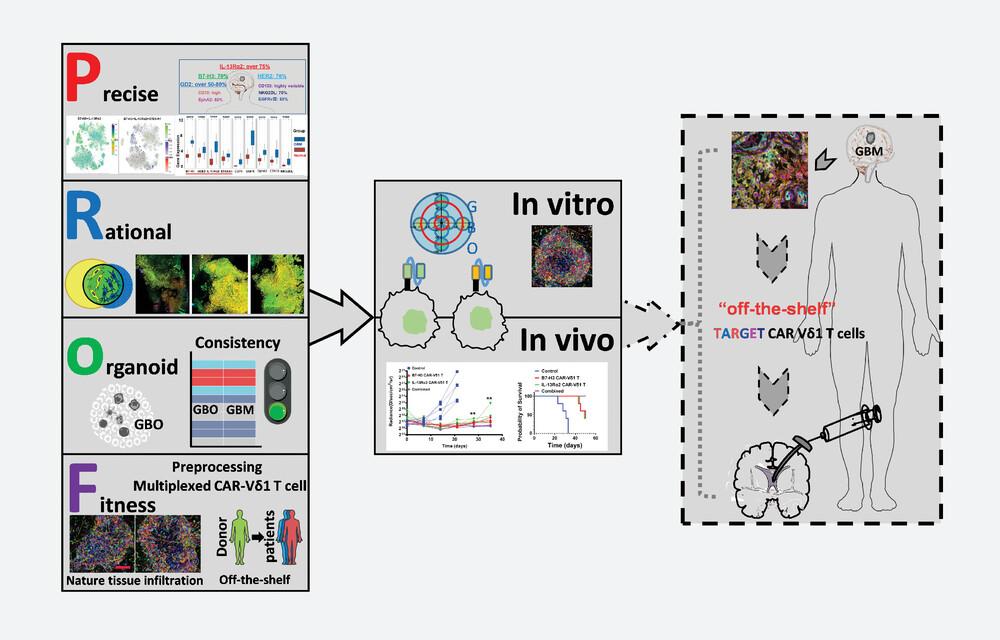
本研究提出的「prof」策略,整合三項核心技術:
- Precise antigen profiling:建立GBM常見抗原庫(target bank),包含 B7-H3、IL-13Rα2、Her2、GD2 等,並透過多重免疫組織化學染色(multiplex IHC)為每位病患量身打造抗原組合。
- Organoid-based evaluation:使用病患衍生的GBOs進行療效預測,確保CAR-T細胞在真實腫瘤微環境中具備殺傷力。
- Fitness of Vδ1 T cells:選用具有天然組織滲透能力的γδ T細胞(尤其是Vδ1亞群)作為CAR載體,並優化其擴增與轉染流程,提升純度與細胞毒性。
🧪 實驗設計亮點
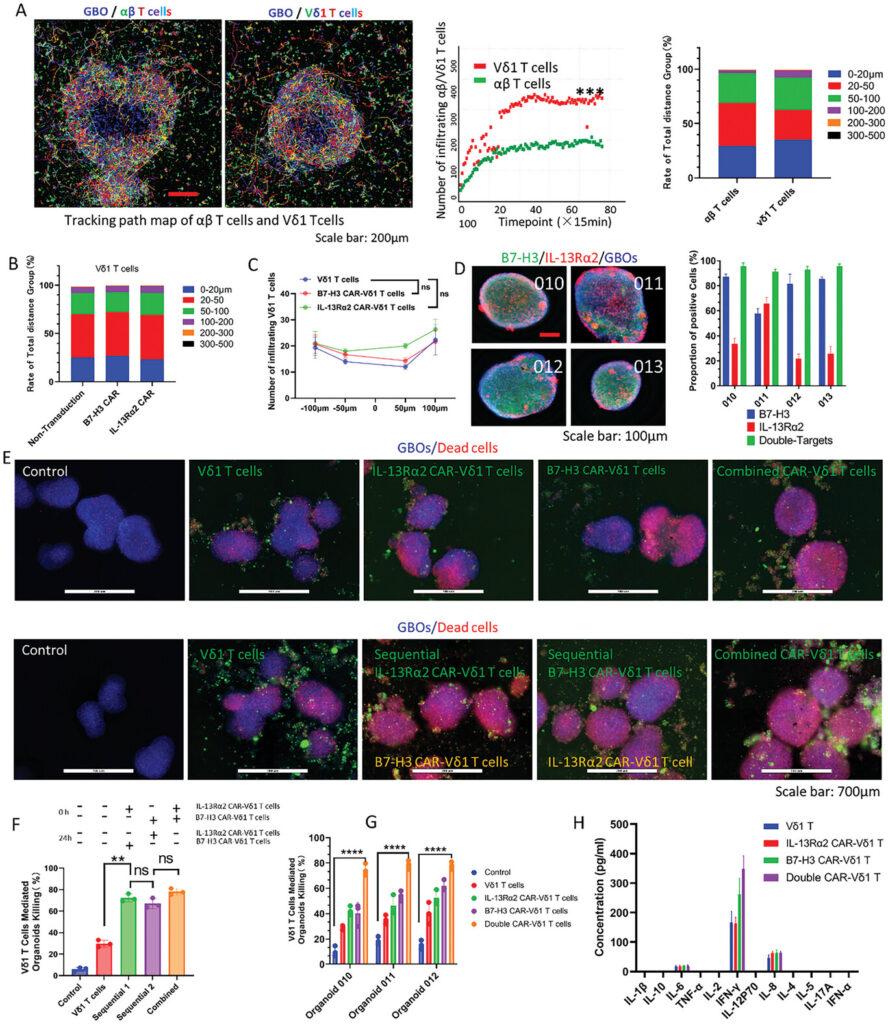
研究團隊從病患手術切除的GBM組織中成功培養出GBOs,並證實其在形態學、基因體與免疫微環境上皆高度模擬原始腫瘤。接著,將工程化的CAR-Vδ1 T細胞與GBOs共培養,發現雙靶點(B7-H3 + IL-13Rα2)與三靶點(+GD2)CAR-T細胞能在48小時內有效清除大部分腫瘤細胞,且細胞表現出低疲憊(exhaustion)與低細胞激素釋放,降低細胞激素風暴風險。
🌱 #Celvivo 在本研究中的角色與培養流程
本研究所使用的GBOs培養流程,採用的是 #微重力三維細胞培養技術(microgravity-based 3D culture),能夠在無需酶解、無外源基質的條件下,直接以腫瘤組織碎片進行培養,保留腫瘤的異質性與免疫細胞組成。具體流程如下:
- 樣本來源:從病患手術切除的新鮮GBM組織取得。
- 培養方式:將組織碎片直接置入專用培養液中,於微重力環境下進行懸浮培養,無需酶解或基質包埋。
- 形成時間:約1–2週內形成圓形腫瘤類器官,存活率高(死亡細胞比例低於10%)。
- 特性驗證:透過組織染色與影像定量 by #TissueFAXS,搭配基因體分析確認GBOs保留原始腫瘤的形態、分子標誌與免疫微環境,包含M2型巨噬細胞與低滲透性T細胞分布。
ClinoStar 提供穩定的微重力環境,促進細胞自然聚集與分化,特別適合用於腫瘤類器官、神經球、心肌球等模型的建立與藥物測試。
📣 結語:從類器官到臨床,個人化免疫療法的未來
本研究不僅展示了多靶點CAR-γδ T細胞在GBM中的潛力,更強調了類器官技術在個人化療法中的關鍵角色。對於台灣正在進行免疫療法、腫瘤模型或細胞治療研究的團隊而言,Celvivo的3D培養平台與GBOs模型,將是不可或缺的工具。
本篇研究使用了流式細胞儀(flow cytometry)、3D球體細胞培養(Celvivo) & 多色組織染色和定量 (TissueFAXS, TissueGnostics),如您有興趣進一步了解以上系統或申請試用,歡迎與我們聯繫,一起推動台灣生醫研究邁向精準醫療的新里程。
Reference:
Rational Design and Organoid-Based Evaluation of a Cocktail CAR-γδ T Cell Therapy for Heterogeneous Glioblastoma. Wang et., al. 2025. Advanced Science.



